| Volltext anzeigen | |
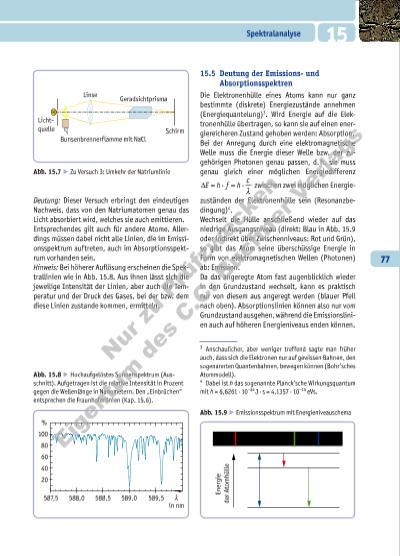
77 Spektralanalyse 15 Deutung: Dieser Versuch erbringt den eindeutigen Nachweis, dass von den Natriumatomen genau das Licht absorbiert wird, welches sie auch emittieren. Entsprechendes gilt auch für andere Atome. Allerdings müssen dabei nicht alle Linien, die im Emissionsspektrum auftreten, auch im Absorptionsspektrum vorhanden sein. Hinweis: Bei höherer Aulösung erscheinen die Spektrallinien wie in Abb. 15.8. Aus ihnen lässt sich die jeweilige Intensität der Linien, aber auch die Temperatur und der Druck des Gases, bei der bzw. dem diese Linien zustande kommen, ermitteln. 15.5 Deutung der Emissionsund Absorptionsspektren Die Elektronenhülle eines Atoms kann nur ganz bestimmte (diskrete) Energiezustände annehmen (Energiequantelung)3. Wird Energie auf die Elektronenhülle übertragen, so kann sie auf einen energiereicheren Zustand gehoben werden: Absorption. Bei der Anregung durch eine elektromagnetische Welle muss die Energie dieser Welle bzw. der zugehörigen Photonen genau passen, d. h. sie muss genau gleich einer möglichen Energiedifferenz ∆E h f h c= =· · λ zwischen zwei möglichen Energie zuständen der Elektronenhülle sein (Resonanz bedin gung)4. Wechselt die Hülle anschließend wieder auf das niedrige Ausgangsniveau (direkt: Blau in Abb. 15.9 oder indirekt über Zwischenniveaus: Rot und Grün), so gibt das Atom seine überschüssige Energie in Form von elektromagnetischen Wellen (Photonen) ab: Emission. Da das angeregte Atom fast augenblicklich wieder in den Grundzustand wechselt, kann es praktisch nur von diesem aus angeregt werden (blauer Pfeil nach oben). Absorptionslinien können also nur vom Grundzustand ausgehen, während die Emissionslinien auch auf höheren Energieniveaus enden können. 3 Anschaulicher, aber weniger treffend sagte man frü her auch, dass sich die Elektronen nur auf gewissen Bahnen, den sogenannten Quantenbahnen, bewegen können (Bohr’sches Atommodell). 4 Dabei ist h das sogenannte Planck’sche Wirkungsquantum mit h = 6,6261 · 10–34 J · s = 4,1357 · 10–15 eVs. Abb. 15.8 E Hochaufgelöstes Sonnenspektrum (Ausschnitt). Aufgetragen ist die relative Intensität in Prozent gegen die Wellenlänge in Nanometern. Den „Einbrüchen“ entsprechen die Fraunhoferlinien (Kap. 15.6). Abb. 15.9 E Emissionsspektrum mit Energieniveauschema Abb. 15.7 E Zu Versuch 3: Umkehr der Natriumlinie 587,5 100 80 60 40 20 % 588,0 588,5 589,0 589,5 in nm λ E ne rg ie de r A to m hü lle Lichtquelle Linse Schirm Geradsichtprisma Bunsenbrennerflamme mit NaCl N u r zu P rü fz w c k e n E ig e n tu m d e s C .C . B u c h n e r V e rl a g s | |
 « |  » |
|
» Zur Flash-Version des Livebooks | |